
La muerte mece la cuna: Muerte súbita en recién nacidos y niños pequeños
La muerte súbita cardíaca ha sido uno de los enigmas más aterradores de la medicina a lo largo de la historia, representando un enorme desafío médico y social. Se define como un colapso total e inesperado que ocurre en menos de una hora desde el inicio de los síntomas en una persona aparentemente sana.
El descubrimiento del síndrome de Brugada a finales del siglo XX, identificado como una de sus causas más frecuentes, ha representado un hito que transformó la cardiología moderna.
Una aproximación histórica a la muerte súbita – La humanidad siempre ha intentado explicar por qué personas jóvenes y fuertes morían repentinamente, en muchos casos sin aviso previo.
En el Papiro de Ebers (1500 a.n.e.), uno de los tratados médicos más antiguos del mundo se describe claramente el cuadro: «Si un paciente tiene dolor en su brazo y lado izquierdo del pecho, hay un riesgo inmediato de muerte». También menciona que existe este riesgo cuando el corazón «tiembla» y tiene «poco poder», una descripción que los historiadores asocian con la insuficiencia cardíaca y probables arritmias graves. Se documenta, además, el uso de la planta digital (un tema aún debatido).
En la Medicina Tradicional China, desde la antigüedad, el principio de «un pulso irregular y sin vida» predecía la muerte inmediata, englobándose dentro de los llamados «pulsos de muerte o terminales».
Hipócrates (400 – 370 a.n.e.) fue el primero en documentar clínicamente la muerte súbita. En sus aforismos afirmó: «Aquellos que sufren de desmayos frecuentes y severos sin causa obvia, mueren súbitamente». Esta observación vinculó por primera vez el síncope con el riesgo fatal inminente. También señaló que «un dolor intenso en el pecho, la clavícula y el dorso, es un signo de mal pronóstico».
La primera ilustración gráfica de muerte súbita conocida es de la Grecia clásica y se encuentra en una piedra sepulcral con el cuerpo de Pheidippides (o Phillipides), el corredor portador de noticias que murió tras correr de Maratón a Atenas.
Durante la Edad Media y el Renacimiento, la muerte súbita (mors repentina) se interpretaba a menudo bajo un prisma religioso o supersticioso. A veces se veía como una bendición (morir sin sufrimiento) y otras como un castigo (morir sin la extremaunción).

Una ilustración notable de este periodo es la muerte del conde Gastón de Foix en el siglo XIV, quien antes de morir repentinamente dijo: «Soy un hombre muerto, que Dios se apiade de mí».
El inicio de la comprensión científica– A partir del siglo XVIII, la medicina comenzó a arrojar luz sobre este fenómeno.
Giovanni María Lancisi (1707): Médico del papa Clemente XI y mente brillante, realizó en su obra De Subitaneis Mortibus una de las primeras investigaciones epidemiológicas tras una «epidemia» de muertes súbitas en Roma. Mediante autopsias, descartó causas sobrenaturales y atribuyó las muertes a causas cardíacas (dilatación ventricular, aneurismas), sentando las bases del método anatomoclínico. Describió signos precursores como palpitaciones, síncope y dolor torácico (una descripción temprana de la angina de pecho), e incluso adelantó la idea de la herencia genética.
Durante este siglo XVIII el médico inglés William Heberden, describió definitivamente la angina de pecho, y a finales del siglo XIX Albert von Bezold demostró, en modelos animales, que la oclusión experimental de las arterias coronarias podía provocar parada cardiaca súbita y fallos en la contracción. También describió el reflejo de Bezold- Jarisch que se desencadena en los infartos de miocardio, sobre todo de cara inferior o diafragmática (zona más rica en receptores sensoriales) y que consiste en una respuesta vasovagal o parasimpática excesiva con bradicardia, hipotensión y vasodilatación periférica. William Heberden: Describió definitivamente la angina de pecho.
A finales del siglo XIX, la ciencia comenzó a entender que el corazón no era solo una bomba mecánica, sino un órgano eléctrico. Así, John MacWilliam en 1889 propuso una teoría revolucionaria: la muerte súbita no era siempre un paro cardíaco en relajación o diástole, sino consecuencia de una tormenta eléctrica caótica denominada fibrilación ventricular. Demostró que “la estimulación eléctrica anormal podía hacer que el corazón dejara de bombear sangre eficazmente”.
El corazón eléctrico y los avances del Siglo XIX y XX – A finales del siglo XIX, la ciencia comenzó a entender que el corazón no era solo una bomba mecánica, sino un órgano eléctrico. Se pueden destacar algunos descubrimientos clave en electrofisiología:
Luigi Galvani (1791): Inventó el galvanómetro para medir la intensidad de la corriente eléctrica.
Rudolf von Koelliker y Heinrich Müller (mediados s. XIX): Demostraron que la contracción del corazón de una rana producía una corriente eléctrica.
Augustus D. Waller (1887): Registró el primer electrocardiograma humano en el St. Mary’s Medical School de Londres. El paciente debía meter las manos en cubos de solución salina conectados a un electrómetro capilar.

El primer electrocardiograma humano diseñado por el fisiólogo Augustus D. Waller, en 1887. Para hacerlo, el paciente metía sus manos en dos cubos de solución salina, conectados con los polos de un electrómetro capilar de Lippman.
Willem Einthoven: Con su galvanómetro de cuerda, hizo posible el registro confiable y sencillo del electrocardiograma (ECG).
John MacWilliam (1889): Propuso una teoría revolucionaria: la muerte súbita no era siempre un paro en relajación (diástole), sino consecuencia de una tormenta eléctrica caótica llamada fibrilación ventricular.
Avances en diagnóstico y tratamiento (Siglo XX)
Albert von Bezold: A finales del XIX, demostró en modelos animales que la oclusión de las arterias coronarias podía provocar parada cardíaca. Describió el reflejo de Bezold-Jarisch (bradicardia e hipotensión excesiva en infartos).
James B. Herrick (1912): Desarrolló el concepto de infarto de miocardio por trombosis y abogó por el uso del ECG para su diagnóstico.
Paul Zoll (1956): Realizó la primera desfibrilación exitosa a tórax cerrado; la muerte súbita pasó a ser reversible.
Mirowski y Mower (1980): Implantaron el primer desfibrilador automático implantable (DAI), iniciando una revolución en la prevención.
A pesar de estos avances, persistía la perplejidad ante un subgrupo de pacientes: jóvenes, deportistas y niños sanos que sufrían muerte súbita y cuyas autopsias revelaban corazones estructuralmente perfectos. Eran consideradas «muertes invisibles».
El descubrimiento del síndrome de Brugada

Los tres hermanos Brugada en 2001.
En 1986, Pedro Brugada, trabajando en Maastricht, atendió a un padre con su hijo de tres años. El niño había sufrido varios síncopes (especialmente con fiebre) y había sido reanimado. Su hermana de tres años había fallecido años antes por fibrilación ventricular con síntomas idénticos, a pesar de tener marcapasos.
Al recuperar los electrocardiogramas de la hermana fallecida, observaron que eran idénticos a los del niño: un patrón extraño en las derivaciones precordiales derechas (V1 a V3) con una elevación del segmento ST que recordaba a una «aleta de tiburón».
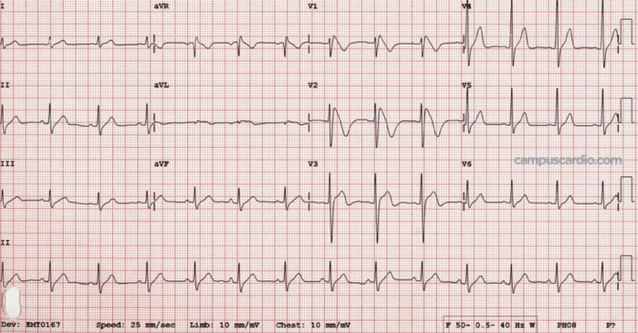
No era un infarto ni un bloqueo de rama; era una huella genética.
El camino a la aceptación fue duro: Pedro y Josep Brugada recopilaron más casos (inicialmente ocho) de pacientes con el mismo patrón ECG y corazones estructuralmente sanos. Tras varios rechazos de revistas que consideraban el hallazgo una «variante normal», publicaron su estudio en 1992 en el Journal of the American College of Cardiology.
Definieron un nuevo síndrome electrocardiográfico-clínico causante de muerte súbita. Aunque la comunidad médica fue inicialmente escéptica, los reportes de casos idénticos en todo el mundo confirmaron que se trataba de una entidad clínica nueva. El tercer hermano, Ramón Brugada, se unió al equipo aportando su experiencia en genética.
En 1998 se incorporaron una serie de descubrimientos genéticos: Se identificó el defecto en el gen SCN5A, que codifica el canal de sodio cardíaco. Aunque hoy se conocen más de 300 mutaciones en 20 genes, el SCN5A sigue siendo el principal responsable (30% de los casos). Esto abrió la puerta al estudio de las canalopatías.
A raíz de la descripción del síndrome, se descubrió que muchas muertes súbitas en el sudeste asiático (conocidas como Lai Tai en Tailandia, Bangungut en Filipinas o Pokkuri en Japón) eran en realidad síndrome de Brugada. En algunos de estos países, es la segunda causa de muerte en hombres jóvenes.

Monumento a la filipina Maria Paz Mendoza-Guazón, quien describió el Bangungut en 1917.
Diagnóstico y Tratamiento actual – En cuanto a la fisiopatología del síndrome de Brugada hay que comprender que las mutaciones en el canal de sodio provocan un mal funcionamiento en la entrada de sodio en las células del ventrículo derecho. Esto crea un desequilibrio eléctrico fatal, especialmente durante la fiebre o la estimulación vagal.
El diagnóstico por el electrocardiograma ECG a veces muestra el patrón característico, pero otras veces es normal pero por los antecedentes familiares de muerte súbita de causa desconocida o la propia historia del paciente con síncopes de repetición o la presencia de una fibrilación auricular idiopática en jóvenes, entonces se puede dilucidar el problema con un test farmacológico de provocación con Ajmalina (que bloquea la corriente de sodio): un test positivo con la aparición del síndrome de Brugada después de la administración del medicamento se considera diagnóstica del síndrome en ausencia de otras explicaciones.
El tratamiento actual contempla fundamentalmente dos medidas:
Colocación de un Desfibrilador Automático Implantable (DAI): Es la única medida indiscutiblemente eficaz para prevenir la muerte súbita en pacientes de alto riesgo.
Ablación con radiofrecuencia: Útil en casos seleccionados.
La decisión clínica en paciente de alto riesgo es clara pero en los pacientes de riesgo intermedio o bajo, la decisión de implantar un DAI debe valorarse conjuntamente con el paciente.
El futuro – El desarrollo de la técnica CRISPR-Cas9 (las «tijeras genéticas») ha abierto la puerta a la posible manipulación y curación de enfermedades hereditarias. Esto permitiría corregir el defecto genético de base en lugar de solo tratar sus consecuencias, como hace el tratamiento actual, además de facilitar el diagnóstico genético preimplantacional en la fertilización in vitro.

“Aquellos que van a estudiar Medicina, y los médicos jóvenes, deberían encender sus antorchas con el fuego de los antiguos” – Rokitanski
Referencias principales
- Brugada P, Brugada J, Brugada R. En búsqueda del secreto de la muerte súbita: el síndrome de Brugada. En: Contribuciones de la medicina española al mundo. Ed EDAF. 2005; 28: 871-887.
- Brugada P, Brugada J. Right bundle branch block, persistent ST segment elevation and sudden cardiac death: a distinct clinical and electrocardiographic syndrome. A multicenter report. J Am Coll Cardiol, (1992), 20 pp. 1391-6.
- Bayes de Luna A y cols. Muerte súbita. Rev Esp Cardiol. 2012; 65(11): 1039-1052.
- Carmona Puerta R. Síndrome de Brugada: Desde los genes hasta la terapéutica. CorSalud. 2010; 2(2): 145-161.
- Sieira J, Asmundis C, Bruguera P. Síndrome de Brugada: 30 años de aventura científica. Rev Esp Cardiol. 2022; 75(12): 988-991.
Deja un comentario